İNDOL
I.-Prensip
İndol, triptofan aminoasidinin hidrolizi ve deaminizasyonu sonucu meydana gelen ürünlerden biridir. Triptofanaz enzimi bulunan bakteri triptofanı parçalayarak indol, pirüvik asit ve amonyağın oluşmasına neden olmaktadır. Bakterinin triptofandan indol oluşturup oluşturmadığı triptofan test besiyerinde ayıracın damlatılmasını takiben yüzeyde kırmızı halkanın oluşup oluşmaması ile konur. İndol oluşumu enterik bakterilerin tanımlanmasında önemli bir test olup özellikle Escherichia coli’yi (pozitif) Klebsiella, Enterobacter, Hafnia ve Serratia türlerinden (büyük bir çoğunluğu negatif) ayırmak için kullanılmaktadır. İndol testinde besiyerinde oluşan indol, Kovac ayıracında bulunan p-dimetil aminobenzaldehid ile birleşerek besiyeri yüzeyinde kırmızı indol halkasının oluşmasına neden olmaktadır. Ayıraç olarak Kovak ayıracı yada Ehrlich ayıracı kullanılabilmektedir. Ehrlich ayıracı nonfermenter basiller veya anaeroblar gibi indol oluşumunun az olduğu bakterilerde daha duyarlıdır.
II.-Besiyerleri ve Ayıraçlar
| A-Triptofan besiyeri (%1 triptofan) | |
| Pepton veya triptycase | 2 g |
| Sodium chloride | 0,5 g |
| Distile su | 100 mL |
| pH 7,2 +/- 0,2 olarak ayarlanır. | |
| B-Kovac ayıracı | |
| Saf amyl veya izoamyl alkol | 150 mL |
| p-dimetilaminobenzaldehid | 10 g |
| Konsantre HCl | 50 mL |
| C-Ehrlich ayıracı | |
| p-dimetilaminobenzaldehid | 2 g |
| Etil alkol | 190 mL |
| Konsantre HCl | 40 mL |
Ayıraçlar hazırlanırken, p-dimethylaminobenzaldehyde alkole eklenip çözünmesi sağlanır. Üzerine asit eklenir.
III.-Kalite Kontrol
A. Pozitif kontrol: Escherichia coli
B. Negatif kontrol: Klebsiella pneumonia
IV.-Yöntem
Test edilecek bakterinin taze kültüründen bir koloni alınarak indol test besiyerine ekimi yapılır. Bir gece 35ºC’de inkübe edilir. İnkübasyon sonrası besiyerine 1-2 damla Kovac veya Ehrlich ayıracı damlatılır.
V.-Sonuçların Değerlendirilmesi

Ayıracın damlatılmasını takiben besiyeri yüzeyinde meydana gelen kırmızı halka testin pozitif olduğunu, diğer bir deyişle bakterinin triptofanaz enzimine sahip olduğunu göstermektedir. Besiyeri yüzeyinde meydana gelen sarı halka ise testin negatif olduğunu göstermektedir.
Metil Red
I.-Prensip
Glikozu fermente edebilen bakteriler glikozdan piruvat oluşumunu takiben piruvatı iki alternatif yoldan metabolize ederler. Bakteri karışık asit fermentasyon yolağını kullanıyorsa, reaksiyon sonunda karışık asit olarak nitelendirilen laktik, formik ve asetik asit oluşmaktadır. Oluşan karışık asitler ortam pH’sının 4.4’ün altına düşmesine neden olur. Test sonuçlarının değerlendirilmesinde kullanılan metil kırmızısı ayıracı bir pH indikatörü olup, pH 4.4 ve altında kırmızı renge dönüşmekte, daha yüksek pH değerlerinde sarı renkte görülmektedir. Enterobacteriaceae ailesi üyelerinin büyük bir bölümü inkübasyon döneminin ilk safhasında ortamdaki pH’yı 4.4’e düşürecek kadar asit oluşturabilirler. Ancak uzayan inkübasyon dönemi sonunda (48-72 saat) besiyerindeki pH tampon sisteminden etkilenmeyen bakteriler gerçek metil kırmızısı testi pozitif kabul edilirler. Bu nedenle test sonuçları 48-72 saat sonunda değerlendirilmektedir.
II.-Besiyerleri ve Ayıraçlar
| A- Metil kırmızısı/ Voges-Proskauer besiyeri | |
| Polipepton | 7 g |
| Glikoz | 5 g |
| Dipotasyum fosfat | 5 g |
| Distile su | 1 L |
| pH 6.9 +/- 0,2 olarak ayarlanır | |
| B-Metil kırmızısı pH indikatörü | |
| Metil kırmızısı | 0,1 g |
| Etil alkol, %95 | 300 mL |
| Distile su | 200 mL |
III.-Kalite Kontrol
A. Pozitif kontrol: Escherichia coli ATCC 25922
B- Negatif kontrol: Enterobacter aerogenes ATCC 13048
IV.-Yöntem
Test edilecek bakterinin taze ve saf kültüründen 1-2 koloni alınarak 2-3 mL besiyeri içeren tüplere ekilir. Test tüpleri 35ºC’ de 48 saatten az olmamak üzere 48-72 saat inkübe edilir. İnkübasyon süresi sonunda test tüplerine 4-5 damla metil kırmızısı ayıracı damlatılır.
V.-Sonuçların Değerlendirilmesi

Bakterinin glikozu karışık asit fermentasyon yolağından metabolize etmesi koşulunda ortam pH’sının 4.4 ve altına düşmesi nedeniyle ayıracın damlatılmasını takiben besiyerinin rengi sarıdan kırmızıya döner ve test “pozitif” olarak değerlendirilir. Aksi halde besiyeri rengi değişmeden kalır. Bu durumda test “negatif” olarak değerlendirilir.
Voges Praskauer
I.-Prensip
Enterik bakteriler glikozu fermente ederken oluşan pirüvik asidi iki alternatif yolakla metabolize ederler. Bakterinin bu yolaklardan karışık asit fermentasyon yolağını kullanıp kullanmadığı metil kırmızısı testi ile saptanmaktadır. Diğer alternatif yolak ise bütilen glikol yolağıdır. Bu yolağı kullanan bakteriler pirüvik asitten asetil metil karbinolün oluşmasına neden olurlar. Voges-Proskauer testi bakterinin glikoz fermantasyonunda bütilen glikol yolağını kullanıp kullanmadığının değerlendirilmesinde kullanılan bir testtir. Asetil metil karbinol oksijen ve %40 potasyum hidroksit varlığında oluşan diasetil hale dönüşür. Besiyerine eklenen α-naftol katalizör görevi görerek besiyeri rengini değiştiren kırmızı rengin oluşmasını sağlar.
II.-Besiyerleri ve Ayıraçlar
| A- Metil kırmızısı/ Voges-Proskauer besiyeri | |
| Polipepton | 7 g |
| Glikoz | 5 g |
| Dipotasyum fosfat | 5 g |
| Distile su | 1 L |
| pH 6.9 +/- 0,2 olarak ayarlanır | |
| B-Ayıraçlar | |
| B1.- α-naftol | |
| α-naftol | 5 g |
| Etil alkol | 100 mL |
| B2.- Potasyum hidroksit (%40) | |
| Potasyumhidroksit | 40 g |
| Distile su | 100 mL |
III.-Kalite Kontrol
A. Pozitif kontrol: Enterobacter aerogenes ATCC 13048
B- Negatif kontrol: Escherichia coli ATCC 25922
IV.-Yöntem
Test edilecek bakterinin taze ve saf kültüründen 1-2 koloni alınarak 2-3 mL besiyeri içeren tüplere ekilir. Test tüpleri 35ºC’ de 24 saat inkübe edilir. İnkübasyonu takiben bakteri üremiş Voges-Proskauer besiyerinden 1 mL alınarak temiz bir tüpe aktarılır. Üzerine sırasıyla 0.6 mL %5’lik α-naftol ve 0.2 mL %40’lık potasyum hidroksit eklenir. Besiyerinin oksijenle temasını arttırmak için tüp hafifçe çalkalanır. Tüpler sabit bir yerde tutularak 10-15 dakika beklenir ve değerlendirme yapılır.
V.-Sonuçların Değerlendirilmesi
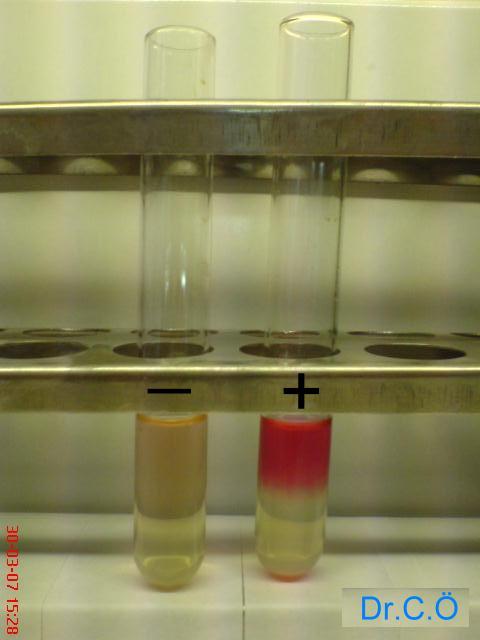
Test tüplerinde asetil metil karbinolün oksidasyon ürünü olan diasetil oluşmuşsa ayıraçların eklenmesini takiben besiyeri kırmızıya döner. Bu koşulda Voges-Proskauer testi “pozitif” olarak değerlendirilir. Besiyerinin renginde bir değişiklik gözlenmediği durumda, test “negatif” olarak değerlendirilir.
Sonuçların değerlendirilmesi ayıraçların eklenmesini takiben en geç 60 dakika içinde yapılmalıdır. Aksi takdirde aslında negatif olan Voges-Proskauer testlerinde oluşan bakır rengi renk değişimi nedeniyle yanlış pozitif sonuçlar elde edilebilmektedir.
Sitrat Kullanımı Testi
I.-Prensip
Sitrat testi, mikroorganizmanın sodyum sitratı, tek karbon kaynağı olarak kullanıp kullanmadığını belirlemek amacıyla yapılır. Simmon sitrat agar besiyeri tüplerde yatık olarak hazırlanır. Bu besiyerinde; nitrojen ve karbon kaynağı olarak protein ve karbonhidratlar bulunmamaktadır. Besiyerinde tek karbon kaynağı olarak sodyum sitrat, nitrojen kaynağı olarak da amonyum fosfat bulunmaktadır. Sitratı kullanabilen organizma aynı zamanda amonyum tuzlarından nitrojenin açığa çıkmasına neden olur. NH3 2+’nin amonyum hidroksite (NH4OH) dönüşmesi besiyerinde alkali ortam oluşur. Besiyerinde bulunan ve pH 6.9’da yeşil renkte olan pH indikatörü renk değiştirerek besiyerinin mavi renge dönüşmesini sağlar. Test yapılırken inokulum miktarının az olmasına dikkat edilmelidir. Yoğun inokülasyon yapıldığında ölen bakterilerin hücre duvarında var olan organik bileşiklerden ortama salınan karbon ve nitrojen yanlış pozitif sonuçların elde edilmesine neden olur. Ayrıca, bilinmeyen bir bakterinin tanımlanması için sitrat testi dışında diğer testler de yapılacaksa bakteri ilk önce sitrat besiyerine daha sonra diğer besiyerlerine ekilmelidir. Bu şekilde diğer besiyerlerinde bulunan protein ve karbonhidratların sitrat besiyerine taşınması engellenmiş olur.
II.-Besiyerleri ve Ayıraçlar
| Simmon Sitrat Besiyeri | |
| Amonyum dihidrojen fosfat | 1 g |
| Dipotasyum fosfat | 1 g |
| Sodyum klorür | 5 g |
| Sodyum sitrat | 2 g |
| Magnesium sülfat | 0,2 g |
| Agar | 15 g |
| Bromtimol mavisi (pH indikatörü) | 0,08 g |
| Distile su | 1 L |
| pH 6.9 +/- 0,2 olarak ayarlanır |
Sitrat kullanım testinde, sitrat besi yeri agar konmaksızın sıvı besi yeri olarak hazırlanabilir. Besiyeri mikroplaka çukurlarına dağıtılacak ise yanlış pozitif sonuçları önlemek amacıyla besi yeri ¼ oranında serum fizyolojik ile sulandırılır.
III.-Kalite Kontrol
A-Pozitif kontrol: Enterobacter aerogenes ATCC 13048
B-Negatif kontrol: Escherichia coli ATCC 25922
IV.-Yöntem
Test edilecek organizmanın saf ve taze kültüründen bir koloni alınarak Simmons sitrat besiyerinin yüzeyine zikzaklar çizilerek ekilir. Test tüpleri 35ºC’de 24-48 saat inkübe edilir.
V.-Sonuçların Değerlendirilmesi

İnkübasyon süresi sonunda, besiyerinin rengi yeşilden maviye dönmüşse bu sonuç “pozitif” olarak değerlendirilir. Bu koşulda bakterinin karbon kaynağı olarak sitratı kullandığı ve oluşan alkali ortam nedeniyle pH indikatörünün renk değiştirdiği gözlenmektedir.
Sitratı karbon kaynağı olarak kullanmayan organizmalar besiyeri pH’sında herhangi bir değişikliğe yol açmadıkları için pH indikatörü renk değiştirmemekte ve besiyeri yeşil renkte kalmaktadır. Bu durumda test sonucu “negatif” olarak değerlendirilmektedir.
