Hydrogen Sulfide (H2S) Oluşumu Testi
I.-Prensip
Bazı bakteriler, enzimatik yolla inorganik sulfurden ya da sülfür içeren aminoasitlerin proteolizi sonucunda H2S oluştururlar. Oluşan bu H2S ’in saptanması iki aşamada gerçekleşmektedir. Birinci aşamada, bakteri besiyeri ortamında bulunan sodium thiosulfate ile reaksiyona girerek sulfite ve H2S oluşturur. İkinci aşamada renksiz olan H2S yine besiyerinde bulunan ferric iyonlar ile birleşerek, ferrous sulfide meydana getirir. Ferrous sulfide, siyah renkte bir çökeltidir. Besiyerinde bu görüntünün saptanması test edilen bakterinin H2S oluşturduğunun işaretidir. Sulfide indikatörü olarak ferrous sulfate, ferric citrate, ferric ammonium sulfate veya citrate kullanılabilir.H2S ’i saptamaya yönelik en hassas besiyerlerinden biri Üç Şekerli Demirli Besiyeri (TSI)’dir. TSI’de %0.1 glukoz, %1 laktoz ve %1 sukroz olmak üzere üç karbonhidrat bulunmaktadır. Bu besiyerinde H2S oluşumunun yanı sıra bakterilerin laktozu kullanıp kullanmadıkları da test edilebilmektedir. Laktozu ve sukrozu fermente etmeyen enterik bakterilerde glukoz fermentasyonuna bağlı olarak gelişen asidik ortam nedeniyle besiyerinde bulunan pH indikatörü renk değiştirerek besiyerini sarı hale getirir. Ancak daha sonra yüzey kısımda proteinlerin oksidatif dekarboksilasyonu sonucu oluşan aminler nedeniyle yüzey pH’sı artar ve yüzey pembe renge döner. Yalnız glikozu kullanan bakterilerde TSI besiyerinin dip kısmı sarı yüzey kısmı ise pembe renkte gözlenir. Glikozun yanı sıra laktoz ve/veya sukrozu da fermente edebilen bakterilerde fermentasyon sonucu oluşan asit besiyeri pH’sını çok düşürür. Yüzeyde proteinlerin oksidatif dekarboksilasyonuna bağlı aminlerin oluşması pH’yı bir miktar attırsada oluşan asitlere bağlı olarak düşen pH’nın üstesinden gelemez Bu nedenle bu tür bakterilere ait TSI besiyerinde hem dip hem de yüzey kısmı sarı olarak gözlenir. Karbonhidratların fermentasyonu sırasında gaz açığa çıkmışsa, gaz oluşumu ya besiyerinin yukarı doğru itilmiş olmasının gözlenmesi ile ya da besiyerinin çatlaması ile tespit edilir. Nonfermenterler gibi her üç şekeri de kullanmayan bakterilerde sadece yüzeyde proteinlerin dekarboksilasyonuna bağlı oluşan alkali ortam nedeniyle besiyerinin yüzeyinin hafif pembeye döndüğü gözlemlenir.
II.-Besiyerleri ve Ayıraçlar
Bu amaçla TSI olarak bilinen üç şekerli demirli besiyeri kullanılabilir.
| Üç Şekerli Demirli Besiyeri | |
| Polypeptone | 20 g |
| Lactose | 10 g |
| Sucrose | 10 g |
| Dextrose | 1 g |
| Sodium chloride | 5 g |
| Ferric ammonium sulfate | 0,2 g |
| Sodium thiosulfate | 0,2 |
| Agar | 13 L |
| Phenol red | 0,025 g |
| Distile su | 1 L |
Besiyerinin pH’sı 7,3’e ayarlanır, otoklavdan çıktıktan sonra tüplere dağıtılır ve yatık olarak soğuması beklenir.
III.-Kalite Kontrol
A- Pozitif kontrol: Salmonella enterica serovar Typhimurium ATCC14028
B- Negatif kontrol: Escherichia coli ATCC 25922
IV.-Yöntem
Test edilecek bakterinin saf ve taze kültüründen iğne öze ile bir koloni alınarak önce besiyerinin dip kısmına batırma yöntemi ile ekilir. Daha sonra besiyerinin yatık kısmına zigzag çizilerek ekim tamamlanır. Besiyerleri 35ºC’de 18-24 saat inkübe edilir.
V.-Sonuçların Değerlendirilmesi

Tiyosülfatın üzerine etki ederek H2S oluşturan bakteriler bu maddenin demir amonyum sülfat üzerine etkisi ile siyah renkli demir sülfit oluştururlar. Besi yerinin dip kısmının siyahlaşması bakterinin H2S oluşturduğu anlamına gelir. Bu koşulda test “pozitif” olarak değerlendirilir. Besi yerinin dip kısmında siyah renk gözlenmediğinde test “negatif” olarak değerlendirilir
Yandaki şekilde TSI besiyerinin farklı reaksiyonları görülmektedir. Siyah renkli besiyerinde H2S oluşmuştur.
Hareket Testi
I.-Prensip
Bakteriler pervane benzeri kamçıları veya diğer organelleri vasıtasıyla hareket ederler. Hareketli bakteriler, sitoplazmik zardan ve hücre duvarını aşarak dışarıya doğru kamçılarını kullanarak hareket ederler. Bakterilerde hareketten sorumlu olan kamçı yani flagel , tek veya birden fazla olabilir. Bakteriler flagellaları dışında kayma, seğirme ve yayılma hareketlerini yaparlar. Bakterinin hareketli olup olmaması uzun yıllardır bakterilerin tanımlanmasında kullanılmaktadır. Flagella basillerde görülmesine karşılık nadiren de olsa bazı koklarda da görülmektedir. Bakterinin hareketli olup olmadığı çeşitli yöntemler ile tanımlanabilir. En basit yöntem özel bir lam kullanarak yapılan asılı damla yöntemidir. Bu yöntemde süspansiyonu yapılan bakteri bir lamele konularak daha sonra test şekilde özel lama yerleştirilir ve mikroskop kullanılarak hareket incelenir. Bir diğer yöntem ise hareket besiyerlerine bakterinin ekilerek incelenmesidir. Hareket test besiyerleri bakterilerin hareketleri saptamak için kullanılır. Sadeece hareket saptamaya yönelik olanları olabildiği gibi hareketin yanında başka özellikleri de aynı anda saptayanları vardır.
Kullanılan besiyerlerine trifeniltetrazolium klorür (TTC) eklenmesi hareketin varlığın saptanmasını kolaylaştırır. Normalde oksitlenmiş formdaki TTC renksizdir. Bakteriler TTC içeren besiyerinde çoğalırken aynı zamanda boyayı içlerine alırlar. Bunun sonucu TTC boyasının dehidrogenazlar ve redüktazlar tarafından indirgenmesiyle elde edilen yapay kromojenik ürün olan formazan oluşur. Orijinal substratın özelliğine bağlı olarak burada oluşan formazan kırmızı renklidir. Hareketin olduğu bölgelere kırmızı renk yayılır.
II.-Besiyerleri ve Ayıraçlar
Bu amaçla çeşitli besiyerleri kullanılabilir.
| Hareket Besiyeri, TTC içeren | |
| Beef extract | 3 g |
| Pancreatic digest of casein | 10 g |
| Sodium chloride | 5 g |
| Agar | 4 g |
| Distile su | 1 L |
| TTC, %1 | 5 mL |
Distile su içine TTC hariç diğer kimyasallar konulur. Agarın erimesi için kaynatılır. Daha sonra TCC %1 eriyiğinden 5 mL eklenir. Tüplere dağıtılarak otoklavda 121°C 15 dakika tutularak sterilize edilir. Otoklavdan çıktıktan sonra soğuması beklenir.
Alternatif olarak Motility-indole-lysine (MIL) Besiyeri, Motility-indole-ornithine (MIO) Besiyeri ve Sulfide-indole-motility (SIM) Besiyeri kullanılabilir.
| MIL Besiyeri | MIO Besiyeri | SIM Besiyeri | |
| Pepton | 10 g | 10 g | 30 g |
| Tripton | 10 g | 10 g | |
| Maya ekstresi | 3 g | ||
| Et ekstresi | 3 g | ||
| Glukoz | 1 g | 1 g | |
| L-lysine hydrochloride | 10 g | ||
| L-ornithine HCl | 5 g | ||
| Ferric ammonium citrate | 0,5 g | ||
| Ferrous ammonium sulfate | 0,02 g | ||
| Sodium thiosulfate | 5 g | ||
| Bromcresol purple | 0,02 g | 0,02 g | 0,02 g |
| Agar | 2 g | 2 g | 3 g |
| Distile su | 1 L | 1 L | 1 L |
III.-Kalite Kontrol
A- Pozitif kontrol: Salmonella enterica serovar Typhimurium ATCC14028
B- Negatif kontrol: Proteus
IV.-Yöntem
Test edilecek bakterinin saf ve taze kültüründen iğne öze ile bir koloni alınarak önce besiyerinin dip kısmına bir cm kalana kadar batırma yöntemi ile ekilir. İğne öze kullanılır ve iğne özenin besiyerine girdiği ve çıktığı hattın aynı olmasına dikkat edilir.Ekim yapılan tüpler 35°C’de 18 saat inkübe edilir.
V.-Sonuçların Değerlendirilmesi
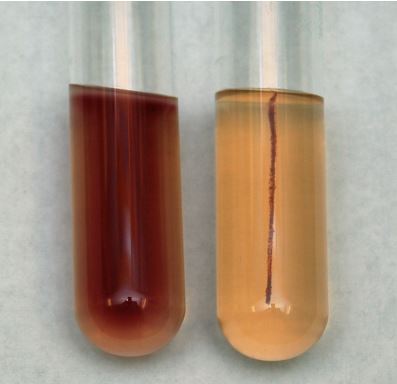
TCC içeren hareket besiyeri değerlendirildiği zaman pozitif olan test sonucunda ekim çizgisinden uzağa uzanan kırmızı bir bulanıklık görülür. Negatif hareket testinde ise kırmızılık ekim hattı ile sınırlıdır.
TCC içermeyen besiyerinde hareketsiz olan bakterinin sadece ekim hattı boyunca çoğaldığı görülmektedir.


MIL besiyerinde hareketliliğe ek olarak indol üretimi, lizin dekarboksilaz ve lizin deaminaz aktivitelerini tespit etmek için kullanılır. Lizin dekarboksilasyonu besiyerinde mor bir
bir renk halinde görülür. Lizin deaminaz besiyerinin en üst 1 cm’sinde kırmızı veya kahverengi kırmızı bir renk halinde görülür. İndol varlığını tesbit etmek için 3-4 damla Kovac reaktifi damlatılmalıdır. Pozitif indol testi Kovac reaktifinin eklenmesinden saniyeler sonra kırmızı renk halinde kendisini gösterir.
SIM besiyeri hareketliliğe ek olarak indol ve hidrojen sülfür üretimini göstermek için kullanılır. İndol varlığını tesbit etmek için 3-4 damla Kovac reaktifi damlatılmalıdır. Pozitif indol testi Kovac reaktifinin eklenmesinden saniyeler sonra kırmızı renk halinde kendisini gösterir. Ekim hattı boyunca siyahlığın görülmesi hidrojen sülfür için pozitif bir test olarak kabul edilir


MIO besiyerinde hareketliliğe ek olarak indol üretimi ve ornitin dekarboksilaz aktivitelerini tespit etmek için kullanılır. Ornitin dekarboksilasyonu besiyerinde mor bir renk olarak
görülür. İndol varlığını tesbit etmek için 3-4 damla Kovac reaktifi damlatılmalıdır. Pozitif indol testi Kovac reaktifinin eklenmesinden saniyeler sonra kırmızı renk halinde kendisini gösterir.
Önemli İpuçları
1.-Ekim için kullanılan iğne öze pürüzsüz olmalıdır.
2.-Test tüplerinde su yoğunlaşmasını engellenmelidir. Bunun için besiyeri içeren tüpler i ekimden önce kapakları gevşetilerek 37oC’de 30 dakika ila 1 saat önceden inkübe edilmelidir.
3.-Negatif sonuçların başka bir yöntem ile teyit edilmelidir.
4.-Bazı bakterilerde hareketlilik yumuşak agar plakalarında daha kolay gözlemlenebilir. Taze dökülmüş yumuşak agar plakalarda agar konsantrasyonu %0,1 ile %0,4 arasında değişir. Bu yöntemin bir avantajı, bulanıklığın çapını ölçerek daha nicel bilgi verebilmesidir. Bir diğer avantajı ise, yayılma kayma ve seğirme gibi diğer kamçı bağımsız hareketleri gösterebilmesidir.
5.-Hareket testi için kullanılabilecek bir diğer besiyeri ise mannitol motility besiyeridir.
6.-Nutrient broth 8 g/L olarak kullanılabilir. Bu besiyerine agar eklenmelidir. İstenirse trifeniltetrazolium klorür (TTC) eklenebilir.
Jelatin Hidrolizi
I.-Prensip
Proteolitik bir enzim olan jelatinaz jelatini hidrolize ederek polipeptitlere ve aminoasitlere dönüştürmektedir. Bu enzim jelatinin yapısını bozarak jelatinin sıvı hale gelmesine neden olmaktadır. Jelatin hidroliz testi özellikle gram-negatif ve gram-pozitif basillerin ayırımında kullanılan bir testtir.
II.-Besiyerleri ve Ayıraçlar
Bu amaçla esculin agar veya esculin buyyon kullanılabilir.
| Besiyeri | |
| Et ekstresi | 3 g |
| Pepton | 5 g |
| Jelatin | 120 g |
| Distile Su | 1 L |
| pH 7,4 +/- 0,2 olarak ayarlanır. |
III.-Kalite Kontrol
A- Pozitif kontrol:Pseudomonas aeruginosa ATCC 10145
B- Negatif kontrol: Escherichia coli ATCC 25922
IV.-Yöntem
Test edilecek bakterinin saf ve taze kültüründen iğne öze ile yoğun bir inokulum alınarak besi yerinin dip kısmına batırılarak yoğun bir ekim sağlanır. Test tüpü ve ekim yapılmamış kontrol tüpü 48 saat 22°C’de, inkübe edilir. İnkübasyon süresi sonunda inkübatörden alınan test ve kontrol tüpleri en az 30 dakika ya da kontol tüpündeki besi yeri tekrar katılaşıncaya kadar buzdolabında bekletilir. Buzdolabındaki bekleme süresi dolunca test tüpleri hafifçe eğik pozisyona getirilerek besi yerinin sıvı hale geçip geçmediği gözlemlenir. Negatif çıkan test tüplerinin iki hafta kadar inkübasyonuna devam edilmelidir.
V.-Sonuçların Değerlendirilmesi
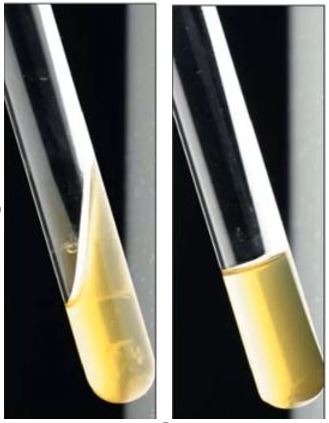
Pozitif test sonucu: Buzdolabında bekletme süresi sonunda kontrol tüpünde bulunan besiyeri tekrar katılaşır. Test tüpündeki besiyerinin kısmen veya tamamen sıvı hale geçtiği gözlemlenir.
Negatif test sonucu: Buzdolabında bekletme süresi sonunda hem kontrol hem de test tüpünde tekrar katılaşma gözlemlenir.
Koagülaz Testi
I.-Prensip
Koagülaz testi, Staphylococcus aureus suşlarını S. epidermidis ve diğer koagülaz negatif türlerden ayırt etmek için yapılır. Test lam ve tüp olmak üzere farklı yöntem kullanılarak gerçekleştirilebilir. Lam testi basittir, kısa bir süre içinde sonuç alınabilir fakat yanlış negatif sonuçlar verebilir. Tüp koagülaz ise testi 24 saate uzayabilen ama daha kesin sonuç veren yöntemdir. Pıhtılaşma hızı bakterinin virülansıyla ilişkili değildir. Koagülaz testinde S. aureus dışında S.schleiferi, S. lugdunensis ve S. intermedius pozitif sonuçlar verebilir. koagülaz için lam testinde pozitif sonuçlar verebilir.
Lam koagülaz testinde bir damla plazma ile bir damla bakteri süspansiyonu cam lam üzerinde karşılaştırılır. Bakteri hücrelerinde bağlı koagülaz varlığında kümeleşme ortaya çıkar. Bakteri hücrelerinde olan MSCRAMM yapışma molekülleri ailesinin bir üyesi olan bir adhezin kümeleşme faktörü görevi yaparak plazmadaki fibrinojene bağlanır ve kümeleşmeyi ortaya çıkarır.
Tüp koagülaz testi, bakteri hücrelerinin küçük bir test tüpünde plazmaya karıştırılmasıyla gerçekleştirilir. Bakteriler plazmada çoğaldıkça staphylocoagulase salgılarlar. Staphylocoagulase, protrombini aktive ederek kan pıhtılaşmasını başlatır. (15). Stafilokoalazı, fibrinojene yapışarak onu fibrine böler ve doğrudan bir fibrin pıhtısı oluşmasına neden olan bir kompleks oluşturur.
II.-Besiyerleri ve Ayıraçlar
| Lam Koagülaz Testi | Tüp Koagülaz Testi |
| Lam | Küçük, kapaklı, steril test tüpü |
| Serum fizyolojik (SF) | Pipet, 0,5 ml damlatılabilir |
| Damlalık, steril olmayan | Pipet ucu |
| Damlalık, steril | Plazma |
| Plazma | Spor |
| Karıştırmak için tahta ve plastik çubuk |
III.-Kalite Kontrol
A- Pozitif kontrol: S. aureus ATCC 12600
B- Negatif kontrol: S. epidermidis ATCC 14990
IV.-Yöntem
Bakteri kültürü taze olmalı ve inhibitör maddeler içermeyen besiyerinde çoğaltılmış olmalıdır. Koyun kanlı agar, çikolata agarı ve trypticase soy agar kullanılabilir. Antibiyotik içeren besiyerleri kullanılmamalıdır.
Plazma olarak liyofilize halde, sitrat veya EDTA ile hazırlanmış tavşan plazması tercih edilmelidir. Plazma üreticinin önerileri doğrultusunda steril ditile su ile sulandırılarak küçük hacımlar halinde steril saklama kaplarına dağıtılmalıdır. Bir hafta içinde kullanılacak ise 4°C derece ısıda buzdolabında saklanabilir. Daha uzun süreli saklanacak ise -20°C derece dondurucular kullanılmalıdır.
- Lam Yöntemi
- 1.-Temiz bir cam lam alınarak iki ucuna birbirinden mümkün olduğu kadar uzakta iki daire çizilir.
- 2.-SF ve EDTA oda ısısına getirilmelidir.
- 3.-Steril olmayan damlalık ile bir damla SF alınarak bir dairenin ortasına damlatılır.
- 4.-Steril olan damlalık ile bir damla plazma alınarak diğer dairenin ortasına damlatılır.
- 5.-Test edilecek bakteri ekili olan petriden yuvarlak öze veya tek kullanımlık çubuk kullanarak 1-2 koloni bakteri alınarak önce SF olan dairenin içine daha sonra plazma olan dairenin içine bakteri aktarılır.
- 6.-Cam lamel “8 hareketi” yapacak şekilde 10 saniye sallanır.
Dairenin birisine bir damla serum fizyolojik diğerine ise plazma damlatılır. lama ılır ve iğne özenin besiyerine girdiği ve çıktığı hattın aynı olmasına dikkat edilir. Ekim yapılan tüpler 35°C’de 18 saat inkübe edilir.
- Tüp Yöntemi
- 1.-Temiz, steril ve kapaklı bir tüp alınarak cama yazar ile işaretlenir ve spora yerleştirilir.
- 2.-Oda ısısına gelmiş olan plazmadan steril pipet ucu kullanarak 0,5 ml alınır ve tüpe aktarılır.
- 3.-Test edilecek bakteri ekili olan petriden yuvarlak öze veya tek kullanımlık çubuk kullanarak 1-2 koloni bakteri alınarak tüp içine aktarılır ve plazma ile karışması sağlanır.
- 4.-Tüpler sporla beraber 35°C’de inkübe edilir.
V.-Sonuçların Değerlendirilmesi
Lam Koagülaz Testi
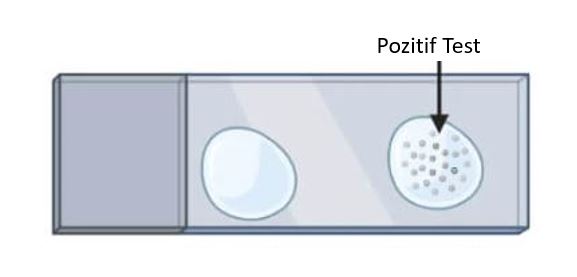
Lam koagülaz testinde SF olan daire içinde kümelenme görülmesi otoaglütinasyonun varlığını gösterir. Test geçersizdir. SF olan daire içinde kümelenmenin olmayıp plazma olan daire içinde olması testin geçerli ve pozitif olduğu gösterir. Her iki daire içinde de kümelenme yok ise sonuç negatif olup tüp testi teyit edilmelidir.
Tüp koagülaz testinde tüpler önce 4 saat sonra pıhtı varlığı açısında incelenir. Var ise pozitif olarak kabul edilir. Yok ise son gözlem 24 saati bulacak şekilde inkübasyona devam edilerek incelenmelidir.
Tüp Koagülaz Testi

LİZİN/ARGİNİN/ORNİTİN DEKARBOKSİLASYONU
I.-Prensip
Dekarboksilazlar, substrata özgül enzimler olup aminoasitin karboksil grubu (COOH) ile reaksiyona girerek aminlerin oluşmasını sağlamaktadır. Bu reaksiyonda oluşan ikinci ürün ise karbondioksittir (CO2). Her aminoasit için özgül bir dekarboksilasyon enzimi bulunmaktadır. Enterobacteriaceae ailesi üyelerinin tanımlanmasında lizin, arginin ve ornitin dekarboksilasyon testleri rutin olarak yapılan testler arasındadır. Dekarboksilasyon sonucu lizinden kadaverin, argininden sitrülin ve ornitinden putresin oluşmaktadır. Dekarboksilasyon enzimi pH 5.5’in altında aktivite göstermektedir. Bu nedenle dekarboksilasyon testinde kullanılan Moeller dekarboksilaz buyyonunun pH’sı 6.0’ya ayarlanır. Üreyen mikroorganizma besi yerinde bulunan glikozu metabolize ederek pH’nın 5.5’e düşmesini sağlar. Dekarboksilasyon testinde, mutlaka aminoasit içermeyen kontrol besi yerinin de kullanılması gerekmektedir. Test ve kontrol tüplerine bakteri inokülasyonu yapıldıktan sonra tüplere mineral yağ konarak anaerop koşullarda inkübasyon sağlanır. İnkübasyon döneminin ilk safhasında her iki tüpte de besi yeri rengi glikoz metabolizasyonu sonucu sarıya döner. Daha sonra aminoasitlerin dekarboksilasyonu sonucu oluşan alkali aminler nedeniyle test tüpündeki besi yeri orijinal mor rengine geri döner. Kontrol tüpü ise dekarboksilasyonun gerçekleşmemesine bağlı olarak sarı renkte kalır.
II.-Besiyerleri ve Ayıraçlar
| Moeller dekarboksilaz besiyeri | |
| Pepton | 5 g |
| Et ekstresi | 5 g |
| Bromkrezol moru | 0.01 g |
| Kresol kırmızısı | 0,005 g |
| Glikoz | 0,5 g |
| Pyridoksal | 0,005 |
| Distile su | 1 L |
| Aminoasit | 2 g |
| L-lizin/L-arginin/L-ornitin (sadece birisi) | 10 g |
| Besiyerinin pH’sı 6,0 +/- 0,2 olarak ayarlanır. |
III.-Kalite Kontrol
| Lizin | Arginin | Ornitin | |
| Enterobacter aerogenes ATCC 13048 | Pozitif | Negatif | |
| Enterobacter cloacae ATCC 13047 | Negatif | Pozitif | Pozitif |
| Klebsiella pneumoniae ATCC 13883 | Negatif |
IV.-Yöntem
Test edilecek mikroorganizmanın taze ve saf kültüründen aminoasit (lizin, arjinin veya ornitin) içeren ve içermeyen iki Moeller dekarboksilasyon buyyonuna ekim yapılır. Besiyerleri üzerine yaklaşık 1cm olacak şekilde mineral yağ eklenerek 35C’ de 18-24 saat inkübe edilir.
V.-Sonuçların Değerlendirilmesi

Kontrol tüpünün sarıya dönmesi, mikroorganizmanın canlı olduğunu ve glikozu fermente ederek dekarboksilasyon enziminin aktivite göstermesi için pH’nın yeteri kadar düştüğünü gösterir.
Aminoasit içeren test tüpünün mavi-mor renge dönmesi aminoasidin dekarboksile olduğunu ve aminlerin oluştuğuna işaret eder. Bu durumda test pozitif olarak kabul edilir.
Test tüpünün sarı olarak kalması durumunda aminoasidin dekarboksile olmadığı anlaşılır ve test negatif olarak değerlendirilir.
LipazTesti
I.-Prensip
Bazı bakterilerde bulunan lipaz enzimi trigliseritleri gliserol ve serbest yağ asitlerine parçalayan bir enzimdir. Enterik bakteriler içinde Cedecea, Proteus, Serratia ve Yersinia cinsi içinde bulunan bakteri türleri değişken olasılıklarla lipaz enzimini içermektedir. Enterik bakterilerin tanımlanmasında kullanılan lipaz aktivitesinin saptanmasında yağ kaynağı olarak mısır yağı kullanılmaktadır. Besi yerinde ayrıca indikatör olarak Victoria blue boyası kullanılır. Bu boya suda çözünebilen mavi renkte bir boyadır. Ancak baz halinde, yağda çözünebilen kırmızı renkte bir boyadır. Besi yeri hazırlanması sırasında pH 7,8’e ayarlanır. Alkali pH’da boya yağ ile karışınca kırmızı renk alır. Besi yerinin soğumasını takiben, boyanın rengi açık pembe-griye döner ve besi yerine bu rengi verir. Eğer test edilen bakteride lipaz enzimi varsa, yağın hidrolizi sonucu yağ asitleri oluşur. Ortam asidik hale gelir ve boyanın rengi pembeden maviye dönüşür
II.-Besiyerleri ve Ayıraçlar
| Lipaz besi yeri (Victoria blue besi yeri) | |
| Pepton | 10 g |
| Maya ekstresi | 3 g |
| Sodyum klorür | 5 g |
| Victoria blue (1:1,500) | 100 mL |
| Agar | 20 g |
| Mısır yağı | 50 mL |
| Besiyerinin pH’sı 7,8 +/-0,2 olarak ayarlanır. | |
| Chrinsten üre agar | 5 L |
| Besiyerinin pH’sı 6,8 +/-0,2 olarak ayarlanır. | 1 g |
Besi yeri manyetik karıştırıcı veya mikser ile homojenize edilerek tüplere dağıtılır. 115°C’de 30 dakika otoklavlanarak steril edilir. Tüpler yatık şekilde dondurulur.
III.-Kalite Kontrol
A- Pozitif kontrol: Serratia marcescens ATCC 13880
B- Negatif kontrol: Escherichia coli ATCC 25922
IV.-Yöntem
Test edilecek bakterinin saf ve taze kültüründen 1-2 koloni alınarak lipaz besi yerine ekim yapılır. Tüpler 24 saat 35ºC’de inkübe edilir.
V.-Sonuçların Değerlendirilmesi

İnkübasyon dönemi sonunda besi yerinin renginin pembeden maviye dönmesi test edilen bakteride lipaz enziminin varlığını gösterir. Bu durumda test sonucu “pozitif” olarak değerlendirilir. Besi yeri renginin açık pembe olarak kalması test edilen bakteride lipaz enziminin olmadığını belirtir. Bu koşulda ise test “negatif” olarak değerlendirilir
